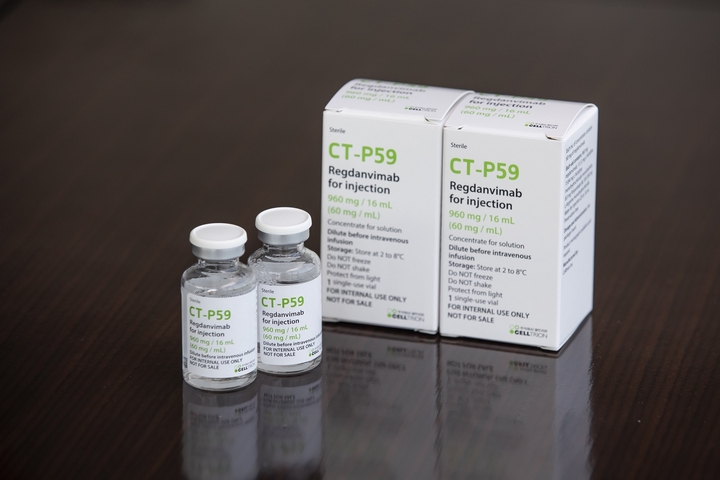
코로나19 국산 치료제 1호가 품목허가를 받았다.
식품의약품안전처(처장 김강립·이하 식약처)는 2월 5일 내·외부 전문가로 구성된 최종점검위원회를 개최하고 ㈜셀트리온이 지난해 12월 29일 허가 신청한 코로나19 항체치료제 ‘렉키로나주’에 대해 3상 임상시험 결과 제출을 조건으로 허가 결정했다고 밝혔다.
특히 ‘렉키로나주’는 국내 개발 의약품으로는 최초로 허가받은 코로나19 치료제이며 전 세계에서 세 번째로 규제당국의 검증을 받은 코로나19 항체치료제라는 점에서 의미가 크다.
식약처 최종점검위원회는 그동안의 식약처 심사결과와 앞서 실시된 두 차례의 자문 내용 등을 종합적으로 점검한 다음 중앙약사심의위원회의 자문의견과 같이 ‘렉키로나주’에 대해 3상 임상시험 결과 제출을 조건으로 품목 허가하는 것으로 결정했다.
‘렉키로나주’는 코로나19 완치자의 혈액에 존재하는 중화항체 유전자를 선별하고 이 유전자를 대량 생산이 가능한 숙주 세포에 삽입(재조합)해 세포 배양을 통해 대량으로 생산하는 유전자재조합 중화항체치료제다.
한편 이날 오전 식약처는 최근 고령자 접종 여부로 논란이 일고 있는 아스트라제네카 코로나19 백신과 관련 만 18세 이상에 허가하되 자료가 충분치 않으므로 만 65세 이상의 접종은 신중히 결정해야 하며, 질병관리청의 예방접종전문위원회에서 논의돼야 한다고 권고하며 판단을 유보했다.