김혜성 이사장(서울치대 졸업, 동대학원 박사)
사과나무의료재단의 이사장이자, 재단 산하 의생명연구소의 미생물 연구자이다.
구강미생물에서 시작해 장내 미생물, 발효 음식의 미생물까지 폭넓게 공부하며 몇 권의 책을 냈고 논문을 발표했다.
『미생물과의 공존』 『입속에서 시작하는 미생물이야기』 『미생물과 공존하는 나는 통생명체다』등 3권이 과학기술부 선정 우수과학도서를 수상했다.
샤워할 때 비누나 여러 세정제를 쓰시나요? 전 쓰지 않습니다. 돌아보면, 샤워할 때 물로만 씻은 지가 30대 초반부터이니 20년은 된 듯합니다. 그렇더라도 전 제 피부의 위생이나 트러블을 걱정하지 않습니다. 오히려 부드러운 제 속살이 만족스럽습니다. 어렸을 적 명절 때나 목욕을 할 수 있었던 때와 달리, 하루 한두 번 따뜻한 물로 몸을 씻을 수 있는 우리 시대에 저는 굳이 비누나 여러 세정제를 써야 할 필요를 느끼지 못합니다.
세정제로 몸에 거품을 가득 내어 씻은 다음 타월로 물을 닦으면 피부가 많이 땅깁니다. 하지만, 세정제 없이 물로만 샤워를 하면 그런 땅김이 훨씬 덜합니다. 세정제에 들어있는 계면활성제, 구체적 성분인 황산라우릴설페이트(SLS : Sodium Lauryl Surfate)에 의한 피부 각질층 손상이 거의 없기 때문이겠죠.
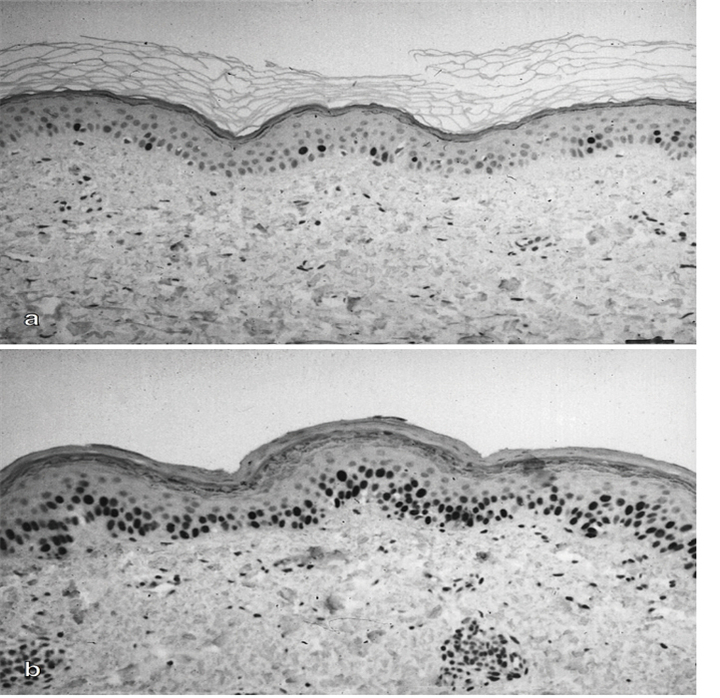
이미 1990년대에 피부를 물에만 노출시킨 경우와 SLS에 노출시킨 경우를 비교한 연구가 있습니다. (Welzel, Metker et al. 1998) 사진에서 보이다시피, SLS에 노출시킨 경우 각질층이 거의 남아있지 않습니다. SLS에 의해 떨어져 나간 겁니다. 당연히 피부가 땅깁니다.
SLS의 작용은 여기서 그치지 않습니다. 아래 시진에서 보이다시피, 외피 하방 진피층의 세포들의 움직임도 많이 달라집니다. SLS에 의해 손상된 외피를 복구하려는 움직임이겠지요. 쥐를 이용한 동물실험은 피부를 SLS 에 노출시키니 보습력이 떨어져 피부에서 수분이 더 증발하고, 면역세포의 사이토카인이 증가함을 보여줍니다.(DaSilva, Sahu et al. 2012) 아토피 같은 피부질환에 노출되기 쉬운 상태가 되는 거죠.
물론, 이런 연구에 쓰이는 SLS의 농도가 우리가 일상에서 노출되는 SLS보다 높다는 지적도 있습니다. 또 세정제로 씻어내고 보습제를 바르면 된다고 생각할 수도 있고요. 하지만, 샤워 중 비눗물이 눈에 들어가면 따가운 느낌이나, 샤워 후 내 피부의 땅김은 일상에서의 SLS 효과가 만만치 않음을 느끼게 합니다. 또 SLS가 아이들 아토피를 비롯해 여러 피부질환의 원인으로 지목된 지는 오래되었고요.
최근 들어 SLS에 대한 주의감이 커진 것은 바로 미생물 때문입니다. 과거 미생물 혹은 세균 하면 병을 일으키는 녀석들로만 생각하다가 지금은 내 몸의 상주미생물이 내 몸을 지킨다는 인식이 확산되고 있으니까요. 피부에 대해서도 마찬가지입니다. 피부에 사는 상주미생물이 오히려 우리 몸을 보호할 수 있습니다. 피부에 많이 살면서 항생제 저항세균으로 유명한 황색포도상구균이 피부에 살고 있는 다른 세균과 상호 소통하고 작용하면서 독성도 낮춰지며 온순한 녀석이 된다는 보고도 있으니까요.(Ramsey, Freire et al. 2016)
피부에 대한 세정제의 우려는 실은, 구강에 대한 치약의 우려보다 훨씬 덜 할 수 있습니다. 일단, 피부는 구강점막보다 방어력이 더 강합니다. 피부는 점막에 비해 세포층이 두텁고 각질층이 피부를 방어함에 반해, 구강은, 결합상피 하방에는 반쪽짜리 세포결합(hemidesmosome)이 존재할 정도로 방어력이 약합니다. 게다가 구강에 쓰는 치약의 성분들은 세정제에 비해 더 강할 수 있습니다. 때가 지지 않는 변기 같은 곳을 치약으로 닦아보라는 유투브 동영상이 존재할 수 있는 이유고, 비누가 눈에 들어가면 따가워도 그래도 견딜 만 하지만, 만약 치약이 피부나 눈에 들어간다면 훨씬 자극이 큰 이유이기도 할 겁니다.
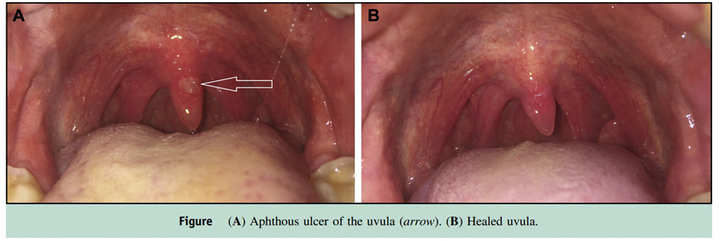
그래서, 이런 치약의 계면활성제는 구강점막의 아토피라 할 수 있는 아프타성구내염(Recurrent Aphthous Stomatitis, RAS)을 더 많이 가져올 수 있다는 지적을 오랫동안 받아왔습니다. 한 증례보고는 치약의 계면활성제로 추정된다는 RAS 임상증례를 보여주기도 합니다.(Pareek and Bhatt 2017) 또 RAS에 대한 SLS의 영향을 종합한 최근의 리뷰논문도 SLS가 구내염이 생길 수 있는 경우나, 지속기간, 통증 등을 더 만들 수 있다 지적하며, RAS 환자들은 SLS가 들어있지 않은 치약을 쓰라고 권합니다.(Alli, Erinoso et al. 2019)
세계적으로 계면활성제를 뽑아 쓰기 시작한 것은 1930년대 들어서입니다. 코코넛 오일에서 뽑은 천연계면활성제가 첫 제품으로 알려져 있습니다. 그러다 1950년대부터는 석유 추출물에서 계면활성제를 뽑아서 가격을 대폭 낮추었고, 이후 계면활성제의 사용은 더욱 확대됩니다. 계면활성제는 건물과 도로와 교량을 닦고, 집과 부엌과 기름 가득 묻은 프라이팬을 닦아 환경위생(sanitation)을 개선시키는데 혁혁한 공헌을 해 온 것이지요. 그러다 점차 계면활성제는 개인위생(hygiene)으로까지 확대되는데 1990년대에는 항균비누나 항균치약까지 나오며 점차 항균력을 강화하고 있는 추세에 있습니다.
환경위생, 혹은 몸 밖 피부의 세정에 쓰일 수 있는 계면활성제가 굳이 몸 안의 구강에까지 쓰일 필요가 있을까요? 구강 역시 당연히 상주 미생물이 살아야 할 공간인데, SLS가 상주미생물총에 좋을 리 없으니까요. 칫솔질은 치주질환을 포함해 여러 전신질환을 일으키는 주범인 구강 내 바이오필름을 제거하고자 함인데, 실은 치약 안에 포함되어 있는 SLS의 바이오필름 제거효과는 미미합니다. 오히려 물리적인 칫솔질이 훨씬 중요한 거죠. 게다가 우리 아이들은 상당량의 치약을 삼키기까지 하는데도 말입니다.
계면활성제가 필요한 경우는 많습니다. 수술실에서라면 당연히 표면과 손을 항균비누로 깨끗이 씻어야겠지요. 하지만, 그 외의 일상에서 계면활성제의 사용은 그 적정선을 넘은 듯 보입니다.
Alli, B. Y., et al. (2019). "Effect of sodium lauryl sulfate on recurrent aphthous stomatitis: A systematic review." 48(5): 358-364.
DaSilva, S. C., et al. (2012). "Increased skin barrier disruption by sodium lauryl sulfate in mice expressing a constitutively active STAT6 in T cells." Archives of dermatological research 304(1): 65-71.
Atopic dermatitis (AD) is a pruritic, chronic inflammatory skin disease that affects 10-20% of children and 1-3% of adults worldwide. Recent studies have indicated that the ability of Th2 cytokines, such as interleukin-4 (IL-4) to regulate skin barrier function may be a predisposing factor for AD development. The present studies examined the ability of increased Th2 activity to affect cutaneous barrier function in vivo and epidermal thickening. Mice that express a constitutively active Signal Transducer and Activator of Transcription 6 (STAT6VT) have increased Th2 cells and a predisposition to allergic inflammation were used in these studies, they demonstrate that topical treatment with the irritant sodium lauryl sulfate (SLS) caused increased transepidermal water loss and epidermal thickening in STAT6VT mice over similarly treated wild-type mice. The proliferation marker Ki-67 was increased in the epidermis of STAT6VT compared to the wild-type mice. However, these differences do not appear to be linked to the addition of an irritant as control-treated STAT6VT skin also exhibited elevated Ki-67 levels, suggesting that the increased epidermal thickness in SLS-treated STAT6VT mice is primarily driven by epidermal cell hypertrophy rather than an increase in cellular proliferation. Our results suggest that an environment with increased Th2 cytokines results in abnormal responses to topical irritants.
Pareek, M. and D. L. J. T. A. j. o. m. Bhatt (2017). "The Wrong Toothpaste and the Painful Burp." 130(1): e19-e20.
Ramsey, M. M., et al. (2016). "Staphylococcus aureus Shifts toward Commensalism in Response to Corynebacterium Species." Frontiers in Microbiology 7: 1230-1230.
Staphylococcus aureus-human interactions result in a continuum of outcomes from commensalism to pathogenesis. S. aureus is a clinically important pathogen that asymptomatically colonizes ~25% of humans as a member of the nostril and skin microbiota, where it resides with other bacteria including commensal Corynebacterium species. Commensal Corynebacterium spp. are also positively correlated with S. aureus in chronic polymicrobial diabetic foot infections, distinct from acute monomicrobial S. aureus infections. Recent work by our lab and others indicates that microbe-microbe interactions between S. aureus and human skin/nasal commensals, including Corynebacterium species, affect S. aureus behavior and fitness. Thus, we hypothesized that S. aureus interactions with Corynebacterium spp. diminish S. aureus virulence. We tested this by assaying for changes in S. aureus gene expression during in vitro mono- versus coculture with Corynebacterium striatum, a common skin and nasal commensal. We observed a broad shift in S. aureus gene transcription during in vitro growth with C. striatum, including increased transcription of genes known to exhibit increased expression during human nasal colonization and decreased transcription of virulence genes. S. aureus uses several regulatory pathways to transition between commensal and pathogenic states. One of these, the quorum signal accessory gene regulator (agr) system, was strongly inhibited in response to Corynebacterium spp. Phenotypically, S. aureus exposed to C. striatum exhibited increased adhesion to epithelial cells, reflecting a commensal state, and decreased hemolysin activity, reflecting an attenuation of virulence. Consistent with this, S. aureus displayed diminished fitness in experimental in vivo coinfection with C. striatum when compared to monoinfection. These data support a model in which S. aureus shifts from virulence toward a commensal state when exposed to commensal Corynebacterium species.
Welzel, J., et al. (1998). "SLS-irritated human skin shows no correlation between degree of proliferation and TEWL increase." 290(11): 615-620.