업계뉴스
전체기사 보기-
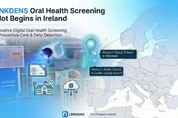
아이오바이오, 아일랜드 학교 기반 아동 구강 스크리닝 파일럿 착수
아이오바이오가 최근 아일랜드 현지 파트너 Diversemart와 협력해 학교 기반 아동 구강 스크리닝 사업의 초기 파일럿에 착수했다. 아이오바이오는 지난 3월 5일 Diversemart와 LinkDens 디지털 운영 플랫폼 도입 및 사업 협력을 위한 LOC를 체결했다. 이어 3월 13일에는 유럽 역내 서버 기반 운영환경을 마련하고, 아일랜드 초등학교를 대상으로 한 초기 파일럿 운영에 들어갔다. 이번 파일럿은 2개 학교를 중심으로 단계적으로 진행된다. 1차 학교는 아일랜드 웩스퍼드(Wexford) 농촌 지역 소재 학교로, 만 5세부터 12세까지 약 90명을 대상으로 한다. 2차 학교는 더블린 샌디마운트(Sandymount) 지역의 공립학교로, 8세·10세·12세 학생 약 190명을 대상으로 운영될 예정이다. 아일랜드에서 추진되는 이번 사업은 보호자 사전 동의와 설문, 현장 표준 촬영, AI 기반 선별 보조, 치과의사 최종 판독, 결과지 자동 생성 및 발송, 중앙 모니터링까지 연결하는 학교 기반 구강 스크리닝 디지털 운영 모델이다. 이를 통해 아동기 구강질환을 조기에 발견하고 예방 습관 형성을 지원하는 한편, 학교 현장의 분산 운영과 중앙 통합 관리가 가능한 공
- 정현중 기자
- 2026-03-20 09:41
-

신흥 DV Friends 종합 카탈로그 발간
㈜신흥이 24번째 ‘DV Friends 종합 카탈로그’를 발간했다. 신흥은 최근 ‘DV Friends 종합 카탈로그’ 통권 제24호를 발간했다고 밝혔다. ‘DV Friends 종합 카탈로그’는 지난 1989년 통권 제1호를 시작으로 발행해 온 종합 상품 카탈로그다. 특히 단순 제품 소개를 넘어, 산업 변천과 트렌드를 조망하는 참고서이자 자료로서 높은 평가를 받아 왔다. 이번 통권 24호는 체계적 분류를 통해 편의성을 한층 강화했다. 카탈로그는 ▲진료용 기기 ▲치과용 임플란트 ▲합금 ▲교정 ▲치과용 기구 ▲근관재료 ▲수복/접착 재료 ▲인상/보철 재료 ▲교합/진단 재료 ▲예방 재료 ▲약품/위생 ▲절삭 연마재 ▲기공 장비 ▲기공 재료 ▲소모품/기타 재료 등 15개 분야로 구성됐다. 신흥은 “DV Friends 종합 카탈로그는 단순 제품 모음집이 아니라 국내 치과 기자재 시장의 현재와 방향성을 담아낸 기록물”이라며 “임상 현장에서 실제로 필요한 정보를 보다 빠르고 정확하게 찾을 수 있도록 이번 호에서는 분류 체계를 더욱 세분화하고 콘텐츠 완성도를 높였다”고 밝혔다. 해당 카탈로그는 신흥 홈페이지 또는 ‘건강한 치과를 만드는 힘 : 덴탈비타민’에서 받아볼 수 있다.
- 천민제 기자
- 2026-03-18 17:18
-

오스템, 기술력 집약 신제품 ‘BDEX 2026’ 최초 공개
오스템임플란트(이하 오스템)가 자사의 기술력을 집약한 신제품 ‘New KS 3’를 이번 주말 부산에서 선보인다. 오스템은 오는 21일과 22일 양일 간 부산 벡스코 제2전시장에서 열리는 ‘부산 치의학 전시회 및 국제학술대회(이하 BDEX 2026)’에 참가, 차세대 임플란트를 공개하며 임플란트 분야에서의 선도적 입지를 확고히 하겠다는 전략을 밝혔다. 오스템은 BDEX 2026의 전체 부스 규모를 전년보다 약 6% 늘려 참가 기업 중 공동 최다 부스로 참여하며 임플란트 관련 핸즈온 부스 및 전시 공간은 5배 이상 확대하는 등 변화를 줬다. 특히 전체 부스의 약 60%를 New KS 3 존으로 구성해 신제품에 대한 몰입도를 한층 강화했다. 부스 상단에는 New KS 3 행잉 배너를 설치하고, 부스 내 대형 스크린을 통해 제품의 핵심 특징을 담은 영상을 상영해 관람객의 시선을 집중시킬 계획이다. 부스 동선 또한 임플란트 중심으로 설계했다. New KS 3 모객 체험 이벤트와 제품 상담, 핸즈온 투어를 부스 전면에 배치해 방문객들이 자연스럽게 신제품을 경험할 수 있도록 했다. 특히 핸즈온 테이블에는 영업 담당자가 상주해 제품 소개와 함께 실제 활용도와 임상적 강점을
- 윤선영 기자
- 2026-03-18 17:16
-

덴티스 ‘루비스’ 노르웨이 공공입찰 수주 성과
덴티스가 최근 메디컬 사업부 수술등 브랜드 ‘LUVIS(루비스)’로 노르웨이 정부 주관 전국 단위 공공입찰(National Tender)을 수주하며 선진국 시장 공략에 의미 있는 성과를 거뒀다. 이번 수주는 ‘Norway National Framework Agreement’ 프로젝트로, 글로벌 의료기기 기업 11개사가 참여한 공개 입찰에서 덴티스가 최종 선정됐다. 덴티스는 데모 장비 공급과 성능 테스트, 현지 평가 등 5개월에 걸친 까다로운 검증 절차를 거쳐 기술력과 품질 경쟁력을 인정받았다. 이번 계약에 따라 덴티스는 루비스 수술등 S250(Mobile·Ceiling·Wall)을 2월부터 순차 공급하며, 향후 3년간 총 180대를 노르웨이 전역 의료기관에 납품할 예정이다. 노르웨이는 의료기기 품질과 안전성 기준이 매우 높은 대표적인 시장으로, 전국 단위 공공입찰 수주는 기술력·신뢰도·공급 안정성을 동시에 검증받았다는 점에서 의미가 크다. 이번 성과는 덴티스 메디컬 사업이 단순 수출을 넘어 구조적 성장 국면에 진입했음을 보여주는 사례로 평가된다. 이에 더해 덴티스는 최근 남아프리카공화국에 최대 규모의 신축 병원을 설립하는 ‘Limpopo Central Hos
- 정현중 기자
- 2026-03-18 17:14
-

루마니아서 AXEL 브랜드 인지도 확대
덴티스가 루마니아 알바이울리아(Theodora Golf Club Alba Iulia)에서 프리미엄 임플란트 ‘AXEL’의 브랜드 인지도를 굳건히 다졌다. 덴티스가 지난 2월 28일 루마니아 알바이울리아에서 ‘AXEL Global Launch Summit’을 개최하며 ‘AXEL’의 글로벌 론칭 행사의 시작을 알렸다. 이번 행사는 AXEL의 글로벌 시장 진입과 브랜드 인지도 확대를 위한 자리로 마련됐으며, 현지 치과의사 및 업계 관계자 약 100여 명이 참석해 높은 관심 속에 진행됐다. 행사에서는 AXEL의 임상적 특성과 설계 디자인 강점을 중심으로 다양한 강연이 진행됐다. Dr. Edmond, Dr. Marcu, Prof. Bran, Dr. Bruno 등 유력 연자들이 참여해 AXEL의 임상 적용 사례와 술식 노하우를 공유하며 참가자들의 관심을 모았다. 특히 본 행사 하루 전에는 Prof. Bran과 함께하는 AXEL 라이브 서저리가 별도로 진행돼 눈길을 끌었다. 현지 핵심 KOL(Key Opinion Leader) 약 10여 명이 참관한 가운데 진행된 라이브 서저리는 실제 수술을 통해 AXEL의 초기 고정력과 임상적 안정성을 확인하고, 즉시 식립 술식에서의
- 정현중 기자
- 2026-03-18 17:12
-

OCP 기반 합성골이식재 미국 FDA 승인
휴덴스바이오가 세계 최초로 OCP(Octacalcium Phosphate) 기반 합성골이식재에 대한 미국 FDA 510(k) 승인을 획득하며 글로벌 의료기기 시장 진출의 중요한 이정표를 세웠다. 이번 승인은 세계 최대 의료기기 시장인 미국에서 제품의 안전성과 유효성을 공식적으로 인정받은 것으로, 국내 생체재료 기술이 글로벌 규제 장벽을 넘어선 사례로 평가된다. 특히 이번 인허가 과정에는 전남대학교 생체재료개발센터(센터장 강성수 교수)의 연구 협력이 중요한 역할을 했다. 전남대학교 생체재료개발센터는 제품의 안전성과 생체적합성을 입증하기 위한 비임상 동물실험 및 생체재료 평가 연구를 수행하며 과학적 근거 확보에 기여했다. OCP는 인체 골 형성 과정에서 중요한 전구체 물질로 알려져 있으며, 체내에서 자연 골조직으로 전환되는 특성을 가지는 차세대 골재생 소재로 주목받고 있다. 그러나 소재 합성의 난이도와 임상적 안전성 입증의 어려움 때문에 실제 의료기기 상용화 사례는 매우 제한적이었다. 휴덴스바이오는 이러한 기술적 난제를 극복하기 위해 수년간의 소재 연구와 공정 개발, 비임상 및 안전성 시험을 진행해 왔다. 특히 소재 합성 기술, 미세구조 제어, 생체반응 검증 등
- 전수환 기자
- 2026-03-18 17:10
-

DOF 구강스캐너 체험 “점심에 만나요”
디지털 덴티스트리 솔루션 전문 기업 디오에프(DOF)가 자체 개발한 구강스캐너 ‘FREEDOM Air’를 앞세워 치과로 직접 찾아가는 방문 데모 프로그램을 운영한다. FREEDOM Air는 일반적인 구강 스캔 기능과 전악 수복(All-on-X)을 위한 포토그래메트리(PIM Solution) 기능을 하나로 통합한 2-in-1 시스템이 특징이다. 특히 145g의 초경량 설계와 넓은 스캔 영역(FOV)을 갖춰 술자의 사용 편의성을 높이고, 고난도 케이스에서도 정밀한 데이터 획득이 가능하도록 설계됐다고 업체 측은 밝혔다. DOF는 신규 장비 도입 시 치과가 느끼는 심리적, 시간적 부담을 덜어주기 위해 체험 중심의 방문 데모 프로그램을 기획했다. 프로그램은 바쁜 치과 일정을 고려해 점심시간에 방문하는 방식으로 진행된다. 방문 후 장비 사용법과 스캔 노하우를 상세히 안내하며, 교육 진행 시 식음료를 제공해 편안한 분위기에서 체험이 이뤄지도록 한다는 설명이다. 나아가 장비 시연은 물론 기공소와 연계를 통한 실제 보철물 제작 결과까지 확인할 수 있도록 지원한다. 이를 통해 실제 스캔 데이터를 바탕으로 제작된 보철물을 직접 확인해 스캔 데이터의 정확도와 디지털 워크플로우의
- 최상관 기자
- 2026-03-18 17:09
-

메가젠, 치과 개원 A to Z 솔루션 ‘눈길’
메가젠임플란트(이하 메가젠)가 치과 개원 준비부터 사후 관리까지 전 과정을 밀착 지원하는 ‘통합 개원 솔루션’을 선보이며 예비 개원의들 사이에서 큰 주목을 받고 있다. 메가젠의 통합 개원 솔루션은 입지 선정부터 자금 계획, 진료 시스템 구축, 인테리어, 복잡한 행정 절차, 내부 경영 시스템 등 개원에 필요한 모든 단계를 전담 매니저가 일대일로 밀착 지원하는 맞춤형 서비스다. 특히 세무, 노무, 법률 자문 등 고도의 전문성이 요구되는 분야에 각계 전문가 그룹과 연계해 차별화된 컨설팅을 제공한다. 개원 후에도 안정적인 경영과 성장을을 돕는 ‘병원 성장 파트너십’까지 함께 제안하고 있다. 솔루션의 핵심은 메가젠만의 ‘1·2·3 차별화 전략’에 있다. 먼저 ‘1대1 개원 지원 서비스’를 통해 입지, 자금, 인테리어, 진료 시스템, 내부 시스템, 허가·신고 등 전 과정을 함께하며 개원 초기부터 안정적인 기반을 마련할 수 있도록 돕는다. ‘2배 더 강한 진료 및 수가 솔루션’을 앞세워 병원의 경쟁력도 높일 계획이다. 진료실의 품격을 높이는 프리미엄 유니트 체어 ‘N2’와 ‘N3’를 비롯해 강도 높은 임플란트 ‘BlueDiamond(블루다이아몬드)’, 치조골 결손을 쉽게
- 최상관 기자
- 2026-03-18 17:08